Patricia Peralta Rodríguez.
Servicio de Anestesiología y Reanimación. Hospital de Parla.
1) Introducción
La osteogénesis imperfecta es una alteración hereditaria del tejido conjuntivo que afecta a la formación del hueso, se caracteriza por fragilidad ósea y masa ósea baja.
Su incidencia es de 1 /20.000 nacimientos y las formas más graves se presentan en 1/50.000 nacidos. En la mayoría de los casos esta enfermedad es causada por una alteración autosómica dominante (1,2), aunque se han descrito casos de herencia recesiva e incluso de mutación espontánea (1). El defecto genético resulta en la sustitución del aminoácido glicina en la cadena del colágeno tipo I, interfiriendo en la estructura helicoidal normal de dicha molécula, componente principal de la piel y huesos (1). Esta interferencia en la síntesis del colágeno tipo I explica la triada clásica de esta enfermedad: facilidad para las fracturas, escleróticas azules y sordera. El diagnóstico se confirma al demostrar la alteración de la síntesis del colágeno en fibroblastos cultivados (1).
La clasificación de Sillence la divide en 4 grupos según su severidad, esta clasificación ha sido recientemente revisada y ampliada (Van Dijk, 2010) El tipo más frecuente es el tipo III.
| Tipo | Severidad clínica | Características típicas | Mutaciones asociadas | Herencia |
| I | Leve no deformante | Codón típicas | Mutaciones asociadas | Herencia |
| II | Severidad clínica | Características típicas | Codón prematuro de terminación en COLIA 1 | AD |
| III | Letal perinatal | Múltiples fracturas de costillas al nacimiento; deformidades significativas; huesos largos anchos; baja densidad radiológica de los huesos del cráneo; esclera oscura | Sustitución en COLIA1 o COLIA2 | Herencia |
| Tipo | Severidad clínica | Características típicas | Mutaciones asociadas | Herencia |
| Tipo | Severidad clínica | Características típicas | Mutaciones asociadas | Herencia |
| Tipo | Severidad clínica | Características típicas | Mutaciones asociadas | Herencia |
| Tipo | Severidad clínica | Características típicas | Mutaciones asociadas | Herencia |
2) Consideraciones preoperatorias
- Sistema cardiovascular.
Se pueden manifestar distintas valvulopatías, siendo la más frecuenta la insuficiencia aórtica, seguido de insuficiencia mitral y prolapso mitral (3) La dilatación de la raíz aórtica también se encuentra con una incidencia ligeramente mayor que en la población general, sin llegar a relacionarse con disección aórtica.
Debido a que la incidencia de estas valvulopatías es baja, no se recomienda la realización sistemática de ecocardiograma salvo exploración física patológica (ej. Soplo cardíaco) ó al alcanzar el paciente la segunda ó tercera década de la vida que es cuando habitualmente comienza la sintomatología.
- Coagulación/diátesis hemorrágica.
Un aspecto importante desde el punto de vista preoperatorio es la incidencia de alteraciones hemorrágicas asociadas a esta enfermedad que oscila entre el 10 al 30%. (1,11). El colágeno defectuoso altera la interacción plaqueta-endotelio y produce un aumento de la fragilidad capilar, así como afectación de la contracción de pequeños vasos después de una lesión y alteración de la agregación plaquetaria. También se ha visto una disminución del antígeno del factor 8 (4, 5). Debido a que estos defectos se relacionan principalmente con fragilidad capilar y alteraciones plaquetarias, los estudios de coagulación preoperatorios suelen ser normales. A pesar de ello, se recomienda realizar analítica con coagulación a los pacientes afectos de OI.
- Sistema Nervioso Central.
Está descrita la impresión basilar, problemas de la unión craneovertebral, incluyendo subluxación atlantoaxoidea e hidrocefalia (6). Entre los síntomas relacionados con esta patología se han descrito cefalea, alteraciones de los pares craneales bajos, hiperreflexia,ataxia, nistagmo, entre otras. No está recomendada de forma rutinaria la realización de una Rx craneocervical a no ser que el paciente presente síntomas. La sordera es una manifestación que se detecta en un 30-60% de los casos, sobre todo en la OI de tipo I,pudiendo ser de conducción o neurosensorial.
- Evaluación de la Via Aérea.
La intubación de estos pacientes puede presentar problemas por varias causas entre ellas la dentinogénesis imperfecta, megalocefalia, macroglosia, cuello corto y limitación para la movilidad. Es necesaria una detallada exploración de la vía aérea preoperatorio.Se recomienda evitar la hiperextensión, para lo cual disponemos de distintos dispositivos (ML, laringoscopio articulado, fibrobroncoscopio)
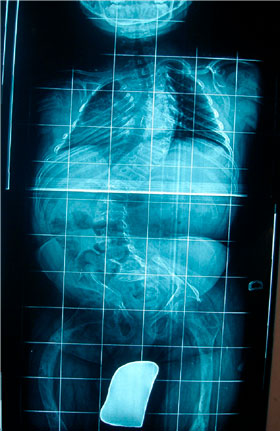
Esta patología también se asocia frecuentemente con cifosecoliosis y otras deformidades torácicas como pectum excavatum y carinatum así como múltiples fracturas costales que deforman el tórax (IMAGEN 1). La escoliosis torácica puede condicionar una disminución de la capacidad vital, así como problemas para la ventilación mecánica. Se considerará por tanto la realización de espirometría/gasometría si la historia clínica del paciente y su exploración así lo aconsejan.
- Alergia al látex.
Los pacientes que sufren esta patología serán sometidos a lo largo de su vida a múltiples intervenciones quirúrgicas, por lo que el riesgo de desarrollar alergia al látex debe ser tomado en cuenta, preparando los quirófanos de manera adecuada (7)
- Tratamiento con bifosfonatos.
El tratamiento de esta enfermedad se basa en tres líneas. Por una parte terapia física y rehabilitadora; por otra intervenciones quirúrgicas para corrección, prevención y tratamiento de fracturas y deformidades; y por último tratamiento farmacológico con bifosfonatos.
La utilización de bifosfonatos para el tratamiento de esta enfermedad se inicia en 1987 con los primeros estudios de Devogelaer (8). Posteriores trabajos han demostrado la mejoría en la calidad de vida de los pacientes con este tratamiento al disminuir el dolor, la incidencia de fracturas y mejorar la movilidad (9). Estas drogas son compuestos nitrogenados (pamidronato, alendronato, ibandronato, entre otros) que inhiben la actividad osteoclástica del hueso, disminuyendo la remodelación ósea y aumentando la densidad mineral (10, 11). El mas extendido en la actualidad es el pamidronato, de uso intravenoso tanto en niños como en adultos. Varios estudios han demostrado que el tratamiento precoz mejora el pronóstico de estos pacientes (12). Entre los efectos secundarios mas frecuentes de este tratamiento se encuentran un síndrome pseudogripal y molestias digestivas inespecíficas (12)
Intraoperatorio
- Traslado del paciente.
Dada la susceptibilidad a sufrir fracturas de estos pacientes, el traslado a la mesa de quirófano debe ser extremadamente cuidadoso. También se debe evitar la
hiperextension de articulaciones.
- Monitorización.
Estándar (TA, ECG, pulsioximetría, capnografía) con PAI/PVC según cirugía y patología del paciente. Es obligatorio monitorizar la temperatura ya que como veremos a continuación estos pacientes presentan una incidencia aumentada de hipertermia transoperatoria.
- Técnica anestésica.
En general, no está contraindicado ningún fármaco. Algunos autores desaconsejan el uso de succinilcolina porque supuestamente las fasciculaciones aumentarían el riesgo de fracturas, aunque existe cierta controversia al respecto. Para el mantenimiento de la anestesia general se pueden usar tanto técnicas de TIVA como balanceada. Se desaconseja el uso rutinario de atropina a menos que sea necesario por su potencial de aumentar la temperatura. La anestesia general no es la única opción para los pacientes con OI; existen casos en la literatura en los que se utiliza la anestesia espinal, la mayoría de ellos en población obstétrica (13).
- Hemorragia intraoperatoria.
Debido a las alteraciones en la hemostasia que como hemos visto previamente pueden presentar estos pacientes, se recomienda una estrecha vigilancia de la cuantía del sangrado quirúrgico. Contamos también con estrategias preventivas, como pueden ser la hemostasia quirúrgica cuidadosa, mantenimiento de la normotermia y el empleo de ciertos fármacos como el ácido tranexámico. En nuestro centro usamos de forma rutinaria este fármaco para pacientes afectos de OI desde el año 2007, encontrando tras su introducción una disminución en los porcentajes de transfusión intra y postoperatoria(umbral transfusional 8g/dl). Pensamos que el uso de ácido tranexámico es al menos en parte responsable de este descenso (TABLA 1)
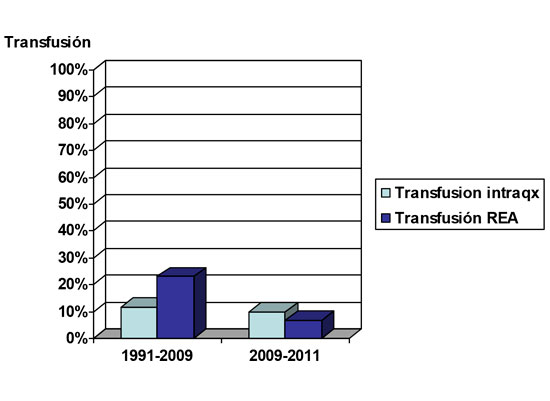
TABLA 1: Evolución del porcentaje de transfusiones a pacientes afectos de OI en el Hospital Universitario de Getafe (introducción del ácido tranexámico en año 2007)
- Hipertermia transoperatoria.
En cuanto a las alteraciones metabólicas, la OI se ha relacionado con hipertermia y acidosis metabólica intraoperatoria. Se considera que a pesar que existe una incidencia mayor de hipertermia perioperatoria en estos pacientes, ésta no se relaciona con la hipertermia maligna (14). Porsborg et al (15), comunican el caso de un niño con OI con un cuadro de hipertermia pero descartan el diagnóstico de maligna con un test de contracción in vitro negativo y ausencia de acidosis metabólica. El estudio de Ghert (14) revisa el curso postoperatorio de 22 niños con OI y lo compara con un grupo control en población pediátrica ortopédica. Los pacientes con OI tuvieron un aumento significativo de la respuesta febril comparado con los del grupo control y se relacionó con la magnitud de la cirugía y la pérdida de sangre sin evidencia de complicación infecciosa (14). Se han postulado varias teorías para explicar este aumento de la temperatura, incluyendo una tasa metabólica aumentada. Se ha asociado con el uso de anticolinérgicos y anestésicos inhalatorios (14). En el caso de presentarse un aumento de la temperatura, se recomienda aplicar una manta con aire frío y en caso de que esto fracase infusión de líquidos fríos y antitérmicos. Si aún asi persiste la hipertermia, debería suspenderse la intervención.
Postoperatorio
- Control del dolor.
Es la complicación más frecuente durante el postoperatorio. Pueden usarse tanto técnicas regionales (bloqueo del nervio femoral, anestesia caudal), como AINEs y/ó opiáceos (cloruro mórfico, Nurse Controlled Analgesia)
- Hemorragia postoperatoria.
Hay que prestar atención a la cuantía del sangrado postquirúrgico ya que el riesgo persiste en este periodo.
- Fiebre sin foco.
Puede presentarse desde horas después de la intervención a 2-3 días después. No se relaciona con infección, sino más bien con una tasa metabólica aumentada, de un modo similar al que ocurre con la hipertermia intraoperatoria.
Conclusiones
La OI es una enfermedad de baja prevalencia que necesita un abordaje multidisciplinario para la mejora en la calidad de vida de estos pacientes. En la literatura se describe variada patología asociada y complicaciones anestésicas y aunque en la práctica clínica no suelen ocurrir con frecuencia (16), el anestesiólogo debe conocerlas para una correcta evaluación preoperatoria y un adecuado manejo intraoperatorio.
Bibliografía
1) Stynowick G, Tobias JD. Perioperative care of the patient with osteogenesis imperfecta. Orthopedics 2007; 30(12): 1044-1049.
2) Antoniazzi F, Zamboni G, Lauriola S, Donadi L, Adami S, Tato L. Early bisphonate treatment in infants with severe osteogenesis imperfecta. J Pediatr 2006; 149: 174-9
3) Bonilla Jiménez V et al. Alteraciones cardíacas en la osteogénesis imperfecta. Estudio ecocardiográfico de casos y controles. MedClin(Barc) 2010.
4) Edge G et al. An unusual manifestation of bleeding diathesis in a patient with osteogenesis imperfecta. European Journal of Anaesthesiology 1997; 14: 215–219.
5) Sperry K. Fatal Intraoperative Hemorrhage During Spinal Fusion Surgery for Osteogenesis Imperfecta. The Americn Journal of Forensic Medicine and Pathology. 1989; 10(1): 54-59
6) Ghert M et al. Increased Postoperative Febrile Response in Children With Osteogenesis Imperfecta. Journal of Pediatric Orthopaedics 2003; 23:261–264.
7) L. Sanchez-Ródenas, J.L. Sanchez Ortega. Anafilaxia intraoperatoria en un paciente con sensibilización al latex desconocida.Rev.Esp. Anstesiol. Reanim. 2005;52:101-104.
8) Devogelaer JP, Malghem J, Maldegue B, Nagant de Deuxchaisnes C. Radiological manifestations of bisphosphonate treatment with APD in a child suffering from osteogenesis imperfecta. Skeletal Radiol 1987; 16: 360-3.
9) Hall RMO, Henning RD, Brown TCK, Cole WG. Anaesthesia for children with osteogenesis imperfecta – a review covering 30 years and 266 anaesthetics. Paediatr Anaesth. 1992; 2:115-121.
10) Fleisch H. Bisphosphonates: mechanisms of action. Endocr Rev. 1998;19: 80-100.
11) Van Beek ER, Cohen LH, Leroy IM, Ebetino FH, Löwik CWGM, Papapoulos SE. Differenciating the mechanisms of antiresorptive action of nitrogen containing bisphosphonates. Bone 2003 ; 33: 805-11.
12) Glorieux F H, Bishop NJ, Plotkin H, Chabot G, Lanoue G, Travers R. Cyclic administration of pamidronate in children with severe osteogenesis imperfecta. N Engl J Med 1998; 339: 947-52.
13) Nakamura M, Yone K, Yamaura I, et al. Treatment of craniocervical spine lesion with Barros F. Caudal block in a child with osteogenesis imperfecta, type II. Paediatr Anaesth. 1995; 5:202-203.
14) Ghert M et al. Increased Postoperative Febrile Response in Children With Osteogenesis Imperfecta. Journal of Pediatric Orthopaedics 2003; 23:261–264.
15) Porsborg et al: Osteogenesis imperfecta and malignant hyperthermia. Is there a relationship? Anaesthesia,1996,vol51,pág.863-865.
16) W. Engel, B. Arrázola, P. Peralta, C. Fernández, C. García Molina, E. Ortigosa. RevEsp Anestesiol Reanim 2011 Mar;58 (3): 151-5. Anesthetic treatment of patients with
osteogenesis imperfecta.